Hukum Termodinamika – Pada pertemuan kali ini ContohSoal.co.id akan menerangkan secara lengkap mengenai materi termodinamika, mulai dari pengertian, hukum, proses, prinsip dan contoh soalnya.Namun dipembahasan sebelumnya ContohSoal.co.id juga telah menjabarkan meteri tentang Termokimia. Nah untuk lebih lengkapnya mari simak aja ulasannya berikut ini.
Pengertian Termodinamika
Termodinamika ialah merupakan sebuah bidang ilmu yang meliputi hubungan di antara panas dan juga jenis energi lainnya. Termodinamika ini sendiri ditemukan dan juga diteliti pada awal abad 18.
Saat itu, terkait dengan dan mendapat perhatiandi dikarenakan penggunaan mesin uap.Pada Termodinamika terdapat dua hukum yang berlaku yakni Hukum Termodinamika I dan Termodinamika II.
Hukum Termodinamika I
“Jumlah kalor yang ada pada suatu sistem ialah sama dengan perubahan energi yang ada di dalam sistem tersbeut ditambah dengan usaha yang dilakukan oleh sistem.”
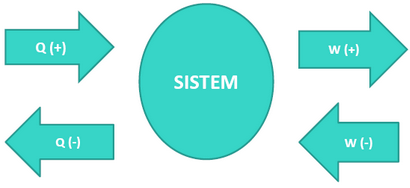
Hubungan antar kalor dan juga lingkungan di dalam hukum I Termodinamika bisa anda lihat pada gambar yang ada di bawah ini.
Energi di dalam sistem ialah jumlah total dari semua energi molekul yang ada di dalam sistem.
Jika sistem melakukan usaha atau pun sistem mendapatkan kalor yang berasal dari lingkungan maka energi yang ada di dalam sistem akan naik, sebaliknya apabila energi yang ada di dalam sistem akan berkurang apabila sistem melakukan usaha terhadap lingkungan atau pun sistem member kalor pada lingkungan.
Dengan begitu kita bisa menyimpulkan jika perubahan energi yang ada di dalam sistem tertutup ialah selisih dari kalor yang diterima dengan menggunakan usaha yang dilakukan sistem.
Rumus Hukum I Termodinamika
| Q=∆U+W | atau | ∆U=Q–W |
Dimana jika diketahui :
∆U = Perubahan energi dalam sistem (J)
Q = Kalor yang diterima ataupun dilepas sistem (J)
W = Usaha (J)
Hukum II Termodinamika
Di bawah ini ialah merupakan bunyi dari Hukum II Termodinamika:
“Kalor bisa mengalir secara alami dari benda yang memiliki suhu panas ke benda yang memiliki suhu lebih dingin; kalor tidak bisa mengalir secara spontan dari benda dingin ke benda panas tanpa dilakukan sebuah usaha”.
Penjelasan Hukum II Termodinamika ialah sebagai berikut ini, silahkan simak ya!
- Tidak akan mungkin membuat mesin yang bisa bekerja di dalam satu siklus, menerima kalor dari satu reservoir serta mengubah kalor seluruhnya menjadi usaha.
- Tidak akan mungkin membuat mesin yang dapat bekerja di dalam satu siklus dengan mengambil kalor dari reservoir yang memiliki suhu rendah dan memberikannya ke reservoir yang memiliki suhu lebih tinggi tanpa adanya usaha dari luar.
- Mesin yang bekerja di antara reservoir suhu Tt dan reservoir suhu Tt (Tt > Tr), memiliki efisiensi yang maksimum.
Prinsip-Prinsip Termodinamika
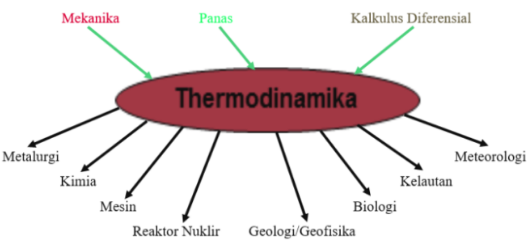
Dalam prinsip penerapan termodinamika yang meliputi Mekanika, pada panas dan Kalkulus Diferensial pada ilmu pengetahuan lain ditunjukkan pada Gambar 1.
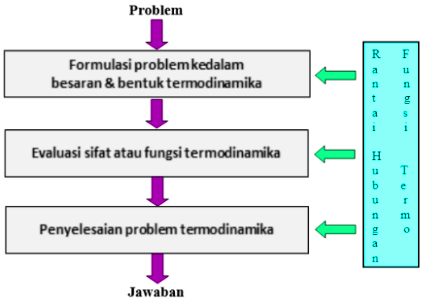
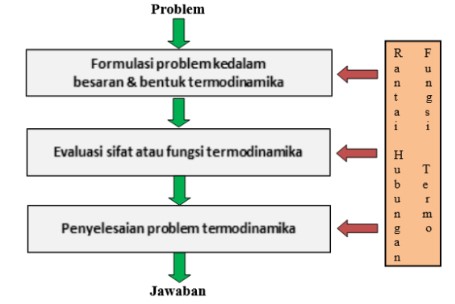
Yang ditunjukan pada Gambar 2 yakni bahwa penyelesaian suatu masalah/problema secara termodinamika dilakukan melalui beberapa tahapan, yakni:
- Formulasi problem ke dalam besaran & bentuk termodinamika. Hal ini yang dikatakan sebagai mengubah bahasa dalam problem ke dalam bahasa termodinamika, kemudian merumuskannya dengan menggunakan besaran-besaran termodinamika.
- Dala termodinamika ada yang namanya evaluasi sifat dan fungsi, yang artinya melakukan analisis terhadap formulasi yang telah disusun pada langkah pertama (1). Tahap ini membutuhkan pemahaman pengetahuan termodinamika yang memadai agar tidak terjadi kesalahan persepsi terhadap arah atau tujuan problema tersebut.
- Penyelesaian problem termodinamika. Pada tahap ini dibutuhkan dukungan pengetahuan matematika/kalkulus (deferensial, integral) sehingga dapat diperoleh jawaban yang valid atau bisa dipertanggungjawabkan.
Maka intinya, dalam prinsip termodinamika yakni sebebnarnya hal yang terjadi secara alami dalam kehidupan sehari-hari. Dengan perkembangan yang terjadi dimana termodinamika direkayasa dengan sedemikian rupa menjadi suatu bentuk mekanisme yang bisa membantu manusia dalam kegiatannya.
Dari perkembangan tersebut diaplikasi termodinamika yang begitu luas ilmu termodinamika sejak abad 17.Kemudian dimulainya pengembangan ilmu termodinamika yakni dengan pendekatan makroskopik ,perilaku umum partikel zat yang menjadi media pembawa energi.
Pengertian Entropi
Entropi bisa diartikan sebagai ukuran ketidakberaturan, di dalam sistem yang tertutup poningkatan entropi oleh penurunan jumlah energi yang tersedia, semakin tinggi entropi maka akan semakin tinggi juga ketakberaturannya.
Entropi Pada Proses Temperatur Konstan
Apabila suatu sistem yang ada pada suhu mutlak T mengalami proses reversible dengan menyerap sejumlah kalor Q maka kenaikan entropi ∆S bisa dituliskan seperti di bawah ini:
∆S = S2 – S1 = Q/T
Penjelasan :
∆S : perubahan entropi (J/K)
S1 : entropi mula-mula (J/K)
S2 : entropi akhir (J/K)
Entropi Pada Proses Temperatur Berubah
Pada proses yang mengalami perubahan temperature, entropi bisa dituliskan sebagai berikut ini:
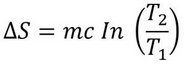
Keterangan :
Penjelasan :
∆S : perubahan entropi (J/K)
S1 : entropi mula-mula (J/K)
S2 : entropi akhir (J/K)
c : kalor jenis (J/kg K)
m : massa (kg)
T1 : suhu mula-mula (K)
T2 : suhu akhir (K)
Contoh Soal Termodinamika dan Pembahasannya
Jika ada suatu mesin memiliki suhu reservoir tinggi 400 derajat Celcius dan suhu reservoir rendah sekitar 70 derajat Celcius, coba hitunglah efisiensi yang ada pada mesin tersebut.
Cara Mengerjakan :
Apabila diketahui :
- Tt = 400°C atau 673 k
- Tr = 70°C atau 343 K
Ditanyakan : η
Maka Jawabannya:
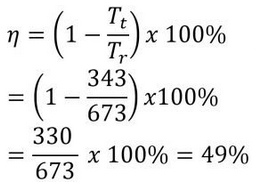
Maka, efisiensi mesin sebesar 49%
Demikianlah materi pembahasan kali ini mengenai termodinamika, semoga bermanfaat.
Pilihan Artikel Lainnya: