Termokimia – Materi pembahasan kal ini masih seputar pelajaran ilmu kimia, yakni tentang termokimia beserta pengertian, persamaan, rumus dan contoh soalnya. Setelah sebelumnya ContohSoal.co.id juga telah membahas materi tentang Contoh Perubahan Kimia. Agar sobat dapat memahami tema pembahasan kali ini mari simak sajian yang sudah ContohSoal.co.id rangkum dibawah ini.
Pengertian Termokimia
Termokimia ialah merupakan suatu ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Namun energi kimia juga dapat didefinisikan yakni sebagai energi yang dikandung setiap unsur atau senyawa.
Kemudian energi kimia yang terkandung pada suatu zat ialah berupa energi potensial, maka pada zat tersebut disebut panas dalam atau entalpi dan dinyatakan dengan simbol H.
Pada entalpi reaktan dan entalpi hasil pada suatu reaksi mempunyai selisih yang disebut perubahan entalpi reaksi dengan simbol ΔH.
Selanjutnya yang merupakan bagian dari ilmu kimia yang mempelajari perubahan kalor atau panas suatu zat yang menyertai suatu reaksi atau proses kimia dan fisika disebut termokimia.
Dengan berdasarkan operasional termokimia mempunyai kaitan dengan pengukuran dan pernafsiran perubahan kalor yang menyertai reaksi kimia, perubahan keadaan, dan pembentukan larutan.
Fokus bahasan dalam termokimia yakni tentang jumlah kalor yang dapat dihasilkan oleh sejumlah tertentu pereaksi serta cara pengukuran kalor reaksi.
Persamaan Termokimia dan Entalpi
Persamaan termokimia ialah merupakan persamaan reaksi setara yang menyertakan kalor reaksi (entalpi reaksi) — yang menunjukkan hubungan antara massa dan energi. Contoh persamaan termokimia:
2H2(g) + O2(g) → 2H2O(g) ΔH= −483,6 kJ
Entalpi, H, yakni fungsi keadaan yang merupakan jumlah dari energi dalam (E) dan hasil kali dari tekanan (P) dan volum (V) sistem.
Kemudian dalam tekanan konstan, pada perubahan entalpi, ΔH, yang terjadi sebuah reaksi disebut juga sebagai entalpi reaksi (ΔHrx) mempunyai nilai yang sama dengan kalor reaksi (q).
- H=E+PV [PKonstan]
- ΔH=ΔE+PΔV [PKonstan]
- ΔH=(qp+w)+PΔV [PKonstan]
- ΔH=(qp+(-PΔV))+PΔV [PKonstan]
- ΔH=qp [PKonstan]
Kemudian pada entalpi reaksi (ΔHrx) ini ialah merupakan suatu fungsi keadaan, yang mana nilainya bergantung pada Hakhir dan Hawal. Dalam suatu reaksi kimia, “akhir” dan “awal” bisa dinyatakan sebagai “produk” dan “reaktan”.
Maka, Hproduk bisa berjumlah lebih atau kurang dari Hreaktan sehingga tanda nilai ΔHrx bergantung pada apakah kalor diserap atau dilepas oleh sistem reaksi.
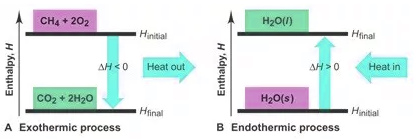
Selanjutnya disebut Reaksi eksoterm yang mana apabila suatu zat melepas kalor sehingga entalpi sistem menurun dan ΔHrx< 0. Maka kesimpulannya Reaksi disebut endoterm jika ia dapat menyerap kalor sehingga entalpi sistem meningkat dan ΔHrx> 0.
ΔHrx= Hakhir – Hawal = Hproduk-Hreaktan
Reaksi Termokimia
Reaksi pada termokimia terbagi atas reaksi eksoterm dan reaksi endoterm yakni sebagai berikut:
Reaksi Eksoterm
Reaksi yang terjadi saat berlangsungnya pelepasan panas atau kalor yang ditulis dengan tanda negatif.
Misalnya:N2(g)+3H2(g)2NH3(g)–26,78Kkal
Perubahan entalpi pada reaksi ini digambarkan sebagai berikut:
- P+Q→R+xKkal
- P dan Q = zat awal
- R =zat hasil reaksi
- x =besar panas reaksi
Menurut hukum kekekalan energi :
Isi panas (P+Q)=isi panas R+xKkal
- H(p+Q)=H(R)+xKkal
- H(R)-H(P+Q)=-xKkal
- ΔH=-Kkal
Reaksi Endoterm
Pada saat berlangsngnya penyerapan panas atau kalor maka Reaksi yang terjadi , yakni suatu perubahan entalpi reaksi bernilai positif.
Misal:2NH3N2(g)+3H2(g)+26,78Kkal
Maka dalam perubahan entalpi pada reaksi endoterm dapat dirumuskan yakni sebagai berikut:
| Rumus | R→P+Q-x Kkal |
| Berlaku | H(P+Q)-H(R)=x Kkal ΔH=xKkal |
Contoh Soal Termokimia
Estimasilah nilai Δreaksi pembakaran berikut dari data energi ikatan rata-rata pada tabel di atas.
Jawab:
ΔH = ∑D(reaktan) − ∑D(produk)
- = [12D(C−H) + 2D(C−C) + 7D(O=O)] –[8D(C=O) + 12D(O−H)]
- =[12(413 kJ)+2(348kJ)+7(495kJ)]–[8(799kJ)+12(463kJ)]
- = 9117 kJ – 11948 kJ
ΔH = −2831 kJ
Nah itulah tadi sajian pembahasan materi tentang termokimia, semoga artikel ini bermanfaat bagi sobat ContohSoal.co.id semua.
Daftar Artikel Lainnya: