Reaksi Eksoterm – Materi pembahasan kali ini masih seputar pelajaran kimia, yakni tentang reaksi eksoterm beserta pengertian, ciri, diagaram dan contohnya. Namun dipertemuan sebelumnya ContohSoal.co.id telah menerangkan materi tentang Termokimia. Untuk lebih jelasnya, maka, simak baik-baik ulasan dibawah ini.
Pengertian Reaksi
Apa yang dimaksud dengan reaksi kimia? ialah merupakan suatu proses alam yang selalu menghasilkan antarubahan senyawa kimia ataupun senyawa-senyawa awal yang terlibat dalam reaksi disebut sebagai reaktan.
Pada umumnya reaksi kimia biasanya diidentikkan dengan perubahan kimiawi, dan akan menghasilkan satu atau lebih produk yang biasanya mempunyai ciri yang berbeda dari reaktan.
Biasanya pada perubahan yang melibatkan pergerakan elektron dalam pembentukan dan pemutusan ikatan kimia, walaupun konsep dasarnya reaksi kimia juga dapat diterapkan pada transformasi partikel-partikel elementer seperti pada reaksi nuklir.
Yang digunakan bersama dalam sintesis kimia untuk menghasilkan produk senyawa yang diinginkan. Dalam biokimia, sederet reaksi kimia yang dikatalisis oleh enzim membentuk lintasan metabolisme, di mana sintesis dan dekomposisi yang biasanya tidak mungkin terjadi di dalam sel dilakukan.
Pengertian Eksoterm
Eksoterm ialah merupakan suatu reaksi kimia yang menghasilkan kalor. Terjadinya rekais ini perpindahan kalor dari system ke lingkungan sehingga lingkungan menjadi lebih panas.
Dalam pembebasan energi reaksi eksoterm akan akan diperlukan sehingga entalpi system berkurang dan perubahan entalpi bernilai negative.
Kemudian pada reaksi pembakaran, misalnya dalam pembakaran kayu, metana, propane, dan reaksi antara serbuk aluminium dan besi oksida merupakan contoh dari reaksi eksoterm.
Contoh lain reaksi eksoterm, yakni reaksi antara kalsium (CaO) dan air. Maka yang dihasilkan dari reaksi tersebut ialah kalsium hidroksida (Ca(OH)2) melalui persamaan reaksi sebagai berikut.
CaO(s) + H2O(l) → Ca(OH)2(aq) + panas
Pada saat pelepasan reaksi ini dapat menyebabkan tangan anda bisa merasakan panas . Nah dalam hal tersebut disebabkan oleh tangan anda (termasuk lingkungan menerima panas dari system yang bereaksi tersebut).
Contoh reaksi eksoterm salah satunya ialah reaksi pembentukan air dari hidrogen dan oksigen sebagai berikut
2H² (g)+O²(g) →2H²O(g)
Ah=-483,6kJ/mol
Ciri-Ciri Reaksi Eksoterm
- Sistem membebaskan energi, umumnya ditandai peningkatan suhu, terlihat api atau jika membutuhkan kalor, ketika kalornya dihentikan reaksi tetap berlangsung
- Entalpi produk lebih kecil daripada entalpi reaksi
- Perubahan entalpi = Hp – Hr < 0, atau bernilai negatif
Diagram Tingkat Energi
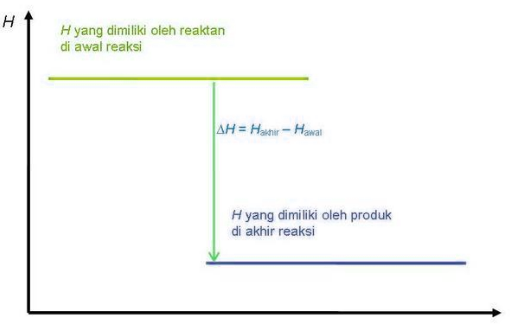
Salah satu cara untuk menunjukkan perubahan kalor/ entalpi yang terjadi dalam suatu reaksi kimia ialah dengan menggunakan diagram tingkat energi.
Pada penulisan diagram energi ini reaktan dan besarnya entalpi yang dimiliki di awal reaksi serta produk dan besarnya entalpi di akhir reaksi. Maka pada selisih entalpi ini akan menunjukkan banyaknya perubahan entalpi yang terjadi.
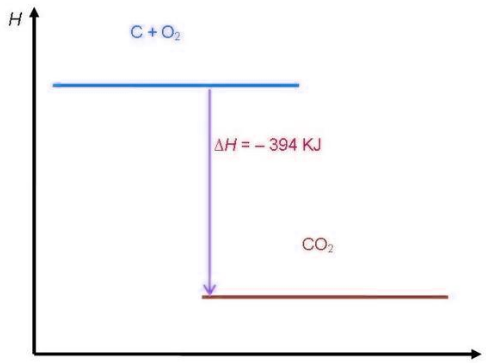
Diagram Energi Reaksi Eksoterm
Pada diagram tingkat energi reaksi eksoterm, entalpi produk lebih rendah daripada entalpi reaktan karena sistem melepaskan kalor ke lingkungan.
Contoh:
Persamaan
digunakan untuk menggambarkan reaksi kimia. Persamaan reaksi terdiri dari rumus kimia atau rumus struktutr dari reaktan di sebelah kiri dan produk di sebelah kanan.
Pemisahan dengan menggunakan tanda panah antara produk dan reaktan (→) yang menunjukkan arah dan tipe reaksi. Ujung dari tanda panah tersebut menunjukkan reaksinya bergerak ke arah mana.
Tanda panah ganda (⇔), yang mempunyai dua ujung tanda panah yang berbeda arah, digunakan pada reaksi keseimbangan. Persamaan kimia haruslah seimbang, sesuai dengan stoikiometri , jumlah atom tiap unsur di sebelah kiri harus sama dengan jumlah atom tiap unsur di sebelah kanan.
Untuk dapat melakukan Penyeimbangan maka kita bisa menambahkan angka di depan tiap molekul senyawa (dilambangkan dengan A, B, C dan D di diagram skema di bawah) dengan angka kecil (a, b, c dan d) di depannya
a A+bB →cC+dD
menggambarkan skema reaksi yang lebih rumit hal tersebut bertujuan guna mengetahui senyawa awal atau akhir, atau juga untuk menunjukkan fase transisi.
Beberapa reaksi kimia juga bisa ditambahkan tulisan di atas tanda panahnya; contohnya penambahan air, panas, iluminasi, katalisasi, dsb. Juga, beberapa produk minor dapat ditempatkan di bawah tanda panah.
Contoh Reaksi Eksoterm
- Reaksi pembakaran
- Reaksi Respirasi
- Reaksi Pembentukan
- Reaksi Nuklir
- Reaksi netralisasi
- Reaksi karbit dengan air
- Reaksi alkana dengan asam
- Reaksi pembentukan molekul dari atom pada fase gas
- Batu kapur direndam dalam air
- Uap air menjadi hujan (kondensasi)
- Pencampuran air basa lemah
- Pencampuran air anhidrat
- Pembantukan air/salju di awan
- Uap air menjadi air
- Air menjadi Es
Nah demikianlah materi pembahasan kali ini mengenai reaksi eksoterm, semoga artikel ini dapat memberi manfaat bagi sobat semua.
Artikel Lainnya: