Hukum Hess – Hay.! sobat ContohSoal.co.id semua.Kali ini ContohSoal.co.id akan membahas materi tentang hess beserta pengertian, bunyi, rumus dan latihan soal secara detail. Namun dipertemuan sebelumnya ContohSoal.co.id juga telah menerangkan materi tentang sifat-kimia. Untuk lebih jelasnya mari langsung aja simak ulasan yang sudah ContohSoal.co.id rangkum dibawah ini.
Pengertian Hukum Hess
Apa yang dimaksud dengan Hukum hess? ialah merupakan suatu hukum dalam kimia fisik untuk ekspansi Hess dalam siklus Hess.
Dalam hukum ini bisa difungsikan guna untuk memprediksi suatu perubahan entalpi dari hukum kekekalan energi (dinyatakan sebagai fungsi keadaan ΔH).
Entalpi ialah merupakan sebauh fungsi keadaan, perubahan entalpi dari suatu reaksi kimia adalah sama, walaupun langkah-langkah yang digunakan untuk memperoleh produk berbeda.
Hukum ini merupakan suatu hubungan kimia fisika yang diusulkan pada tahun 1840 oleh Germain Hess, kimiawan asal Rusia kelahiran Swiss.
Perubahan entalpi suatu reaksi dapat dihitung walaupun tidak bisa di ukur secara langsung. Cara mengukurnya dengan cara melakukan operasi aritmatika di beberapa persamaan reaksi yang perubahannya dapat di ketahui.
Apabila pada suatu persamaan reaksi di kalikan atau di bagi dengan suatu angka, pada perubahan entalpi juga harus di kali atau di bagi. Begitu juga dengan jika persamaan di balik maka perubahan entalpi juga di balik.
Bunyi Hukum Hess
Di bawah ini ialah merupakan bunyi hukum hess:
| Dalam jumlah panas yang dilepaskan pada suatu reaksi kimia tidak tergantung pada jalannya reaksi tetapi ditentukan oleh keadaan awal dan akhir. |
Kegunaan Hukum Hess
Kegunaan hukum ini adalah untuk memprediksi perubahan entalpi dari hukum kekekalan energi yang dinyatakan sebagai fungsi keadaan ΔH.
Hukum tersebut dapat digunakan untuk menghitung jumlah entalpi keseluruhan proses reaksi kimia walaupun menggunakan rute reaksi yang berbeda.
Rumus Hukum Hess
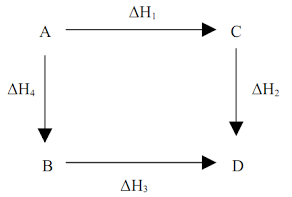
Perhatikan gambar di atas, mereaksikan A dengan D dapat menempuh jalur B dan C. dengan merubah entalpi yang sama (ΔH¹+ΔH²=ΔH³+ΔH4)
Jika perubahan kimia terjadi pada beberapajalur yang berbeda, maka perubahan entalpi pada keseluruhan juga sama. Maka untuk itu ΔH pada reaksi tungga dapat di rumuskan:
| Rumus | ΔHreaksi=∑ΔHf(produk)-∑ΔHf(reaktan) |
Soal Latihan Hukum Hess
90.1kj
C(s)+2H²O(g) CO²(g)+2H²(g)
⇑ ⇑
-483.6kj -393.5kj
C(s)+2H²(g)+O²(g)
Dengan berdasarkan diagramm diatas, maka jelas sudah apabilaC(s)+2H²(g)+O²(g) direaksikan menjadi CO²(g)+2H²(g) mempunyai perubahan entalpi sebesar -393,5kj .walaupun terdapat reaksi dua langkah, tetap saja perubahan entalpi akan selalu konstan (-483,6kj+90,1kj=-393,5kj)
Hitunglah jumlah kalor yang dibebaskan pada pembakaran 1 mol hidrokarbon C²H² (mr=26) jika diketahui entalpi pembentukan H²O(g)=-285kj/mol,CO²(g)=-393kj/mol dan C²H²(g)=+227kj/mol
Pembahasan:
Pertama, hal yang harus dilakukan ialah membuat persamaan reaksi untuk pembakaranC²H². Ingat bahwa pembakaran artinya senyawa direaksikan dengan oksigen(O²).
Dalam reakspembakaran selalu menghasilkan karbondioksida dan uap air. Kemudian disetarakan akan dihasilkan persamaan reaksi seperti berikut:
C²H²+5/2O²(g)→2CO²(g)+H²O
- ΔHreaksi=ΔH hasil-ΔH pereaksi
- ΔHreaksi=2ΔHfCO²+ΔHf H²O-ΔHfC²H²-5/2ΔHf O²
- ΔHreaksi=2(-393)+(-285)-227-5/2(0)
- ΔHreaksi=-1298kj/mol
Ingat bahwa unsur bernilai 0 sehingga ΔHfO²=0
Contoh Soal.2
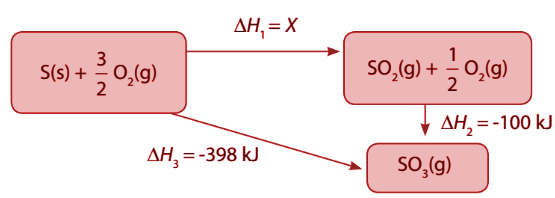
Perhatikan diagram reaksi berikut.
Berdasarkan diagram tersebut, berapakah nilai X?
Pembahasan:
Berdasarkan penemuan Henry Hess, “Pada kalor yang diserap atau dilepaskan dalam suatu reaksi tidak tergantung pada jalannya reaksi, tetapi tergantung pada keadaan awal dan akhir reaksi:
ΔH³=ΔH¹+ΔH²-398=x+(-100)x=-298kj
Jadi, nilai X ialah-298 kJ.
Contoh Soal.3
Simak pada persamaan termokimia dibawah ini:
- 2H²(g)+O²(g)→2H²O(l)ΔH=-136Kkal
- H²(g)+O²(g)→H²O²(l)ΔH=-44,8Kkal
Hitunglah ΔH
untuk reaksi,
2H²O²→2H²O+O²
Pembahasan
Untuk mendapatkan reaksi tersebut, kita gabungkan reaksi pada tahap 1 dan tahap 2 sehingga diperoleh:
2H²+O²→2H²OΔH=136 Kkal
2H²O²→2H²+2O²ΔH=+89,6 Kkal
+
2H²O²→H²OΔH=-46,4Kakl
Jadi, ΔH
untuk reaksi 2H²O²→2H²O+O²
sebesar -46,4 Kkal.
Nah itulah pembahasan mengenai hukum hess, semoga artikel ini dapat bermanfaat bagi sobat semua.
Pilihan Artikel Lainnya: