Isomer – Pada pertemuan sebelumnya kita sudah membahas materi tentang Reaksi Endoterm. Maka materi pembahasan kita kali ini yakni mengenai isomer lengkap beserta pengertian, alkan, optis, struktu, butana dan contoh soalnya. Nah untuk lebih jelasnya simak materi yang sudah ContohSoal.co.id rangkum di bawah ini.
Pengertian Isomer
“Dalam ilmu kimia,Pengertian isomer ialah merupakan molekul-molekul dengan rumus kimia yang sama dan dengan jenis ikatan yang sama, namun mempunyai susunan atom yang berbeda bisa diibaratkan sebagai sebuah anagram”
Kebanyakan isomer mempunyai sifat kimia yang mirip satu sama lain. Juga ada istilah isomer nuklir, yaitu inti atom yang mempunyaitingkat eksitasi yang berbeda.
Contoh sederhana dari suatu isomer yakni C3H8O.
Isomer Struktur
Keisomeran struktur terjadi akibat perbedaan susunan ikatan antar atom ataupun gugus-gugus fungsi dalam suatu molekul. Keisomeran struktur dapat dibedakan menjadi:
Isomer Kerangka
Pada senyawa yang merupakan kerangka mempunyai rumus molekul dan gugus fungsi yang sama, namun kerangka (rantai karbon utama) berbeda. Contohnya, butana dengan rantai utama C4 dan 2-metilpropana dengan rantai utama C3.
CH³-CH²-CH²-CH³
Butana
CH³
⎜
CH²-CH-CH³
2-metilpropana
Isomer Posisi
Kemudian pada senyawa yang termasuk posisi mempunyai rumus molekul dan gugus fungsi yang sama, namun posisi gugus pada kerangka berbeda.
Contohnya, 1-butena dengan 2-butena berbeda posisi ikatan rangkap C=C; dan 1-butanol dengan 2-butanol berbeda posisi gugus hidroksil (–OH).
Isomer Gugus Fungsi
Berikut ini merupakan beberapa pasangan deret homolog yang berisomer gugus fungsi, ialah:
- alkanol (alkohol) dengan alkoksialkana (eter) dengan rumus umum: CnH2n+2O
Contoh : etanol dengan metoksimetana (dimetil eter). - alkanal(aldehida)dengan alkanon (keton) – mepunyai rumus umum: CnH2nO
Contoh gugus fungsi aldehida yakni: propanal dengan propanon. - asamalkanoat (karboksilat) dengan alkil (ester) mempunyai rumus umum: CnH2nO2
Contoh gugus fungsi asam karboksilat ialah: asam propanoat dengan metil etanoat.
Isomer Ruang (Stereoisomerisme)
Keisomeran ruang terjadi akibat perbedaan konfigurasi atau susunan atom dalam ruang. Keisomeran ruang dapat dibedakan menjadi:
Isomer Geometri
Terjadinya keisomern yakni disebakan oleh adanya keterbatasan rotasi bebas pada suatu ikatan dalam molekul. C–C merupakan ikatan tunggal, yang mana atom karbon dapat berotasi bebas terhadap atom karbon lainnya.
Akan tetapi, C=C pada ikatan rangkap dua, dimana rotasi atom karbon cenderung terbatas yakni disebabkan oleh adanya ikatan pi. Jadi, posisi atom atau gugus atom yang terikat pada kedua atom C pada ikatan C=C tidak dapat berubah.
Keisomeran geometri umumnya ditemukan pada senyawa-senyawa dengan ikatan C=C di mana masing-masing atom C mengikat dua atom atau gugus atom yang berbeda.
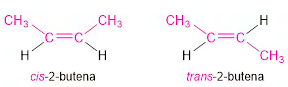
Dengan didasari dari posisi atom atau gugus atomnya, dimana isomer geometri dibedakan menjadi bentuk cis dan bentuk trans.
- Isomer cis ialah isomer di mana atom atau gugus atom sejenis terletak pada sisi yang sama.
- Isomer trans yakni isomer di mana atom atau gugus atom sejenis terletak pada sisi bersebrangan.
Sebagai contoh, cis-2-butena dengan trans-2-butena merupakan pasangan isomer geometri cis-trans.
Isomer Optis
Keisomeran optis terjadi jika senyawa memiliki suatu atom asimetris. Pada senyawa karbon, keisomeran optis terjadi pada senyawa yang mempunyai atom karbon asimetris, yakni atom karbon yang terikat pada 4 atom atau gugus atom yang berbeda.
Apabila posisi ditukarkan dari dua gugus pada atom asimetris , maka akan terbentuk dua molekul berbeda yang merupakan bayangan cermin dari satu sama lainnya.
Kedua molekul ini tidak dapat saling ditindihkan satu sama lain (non-superimposable). Sifat tidak saling tumpang tindih seperti tangan kiri di atas tangan kanan dan sebaliknya disebut sebagai kiral.
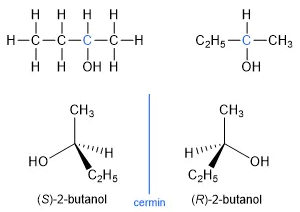
Sebagai contoh, 2-butanol memiliki satu atom karbon kiral yakni atom karbon nomor 2 seperti terlihat pada gambar berikut. Atom karbon tersebut berikatan dengan empat gugus berbeda, antara lain –C2H5, –H, –OH, dan –CH3.
Isomer optis tidak dapat dibedakan berdasarkan sifat-sifat fisis seperti titik didih dan titik leleh, sebagaimana isomer-isomer jenis lainnya yang telah dijelaskan sebelumnya.
Satu-satunya sifat fisis yang dapat membedakan isomer optis ialah sifat optis, yakni merupakan sebuah kemampuan untuk memutar (merotasikan) bidang cahaya terpolarisasi. Maka yang mempunyai kemapuan memutar polarisasi cahaya disebut bersifat optis aktif.
Menurut aturan Le Bel–van’t Hoff, jumlah maksimum isomer optis dari senyawa karbon yang tidak memiliki bidang simetri internal ialah sebanyak 2n, di mana n ialah merupakan jumlah atom karbon kiral.
Contoh Soal Isomer
Pada senyawa berikut tentukanlah apakah mempunyai keisomeran geometris cis-trans.a. 1,2-dikloroetena
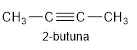
b. 2-butuna
Jawab:
a. 1,2-dikloroetena mempunyai isomer geometri cis-trans sebab terdapat ikatan C=C yang rotasi bebasnya terbatas dan masing-masing atom C pada ikatan C=C tersebut mengikat dua atom yang berbeda, yaitu atom H dan atom Cl.
b. 2-butuna tidak memiliki isomer geometri cis-trans karena bentuk geometri molekulnya yang linear dan masing-masing atom C pada ikatan rangkap tiga hanya dapat mengikat satu gugus atom.
Demikianlah materi pembahasan kali ini tentang isomer, semoga artikel ini dapat bermanfaat bagi sobat semua.
Artikel Lainnya: