Kesetimbangan Kimia – Masih seputar pembahasan mengenai ilmu kimia yakni tentang kesetimbangan kimia dimulai dari pengertian, faktor, pergeseran dan contoh soalnya. Setelah sebelumnya ContohSoal.co.id juga telah membahas materi tentang Reaksi Eksoterm. Nah untuk kelanjutan tema kita kali ini langsung aja simak ulasan dibawah ini.
Pengertian Kesetimbangan Kimia
Kesetimbangan kimia ialah merupakan suatu kondisi dalam reaksi kimia yang reversibel atau dapat balik dimana tidak terdapat perubahan baik jumlah reaktan maupun jumlah produk yang terbentuk dalam reaksi tersebut.
Reaksi reversibel ialah reaksi dimana produk yang terbentuk akan segera bereaksi kembali untuk menghasilkan reaktan awal.
Pada keadaan setimbang, dua reaksi yang berlawanan ini akan terjadi dalam kecepatan yang sama sehingga tidak akan terjadi perubahan jumlah dalam reaktan maupun produknya.
Ketika suatu reaksi mencapai titik ini, maka dapat dikatakan bahwa reaksi tersebut telah selesai. Pada kondisi kesetimbangan tertentu, reaksi dapat mencapai konversi reaktan menjadi produk yang maksimum.
Dalam sistem tertutup, dimana produk hasil reaksi tidak dapat keluar maka akan didapatkan hasil akhir reaksi berupa campuran antara reaktan dan produk reaksi pada kesetimbangan.
Sebagai contoh yakni reaksi berikut :
A ⇋ B + C
Pada keadaan setimbang, reaksi perubahan A menjadi B dan C akan sama cepatnya dengan reaksi antara B dan C untuk membentuk A.
Dalam hal ini reaksi A menjadi B dan C merupakan reaksi maju dengan laju reaksi 1 sedangkan reaksi B dan C menjadi A merupakan reaksi balik dengan laju reaksi 2 dimana kedua laju reaksinya sama.
Rumus Umum Kesetimbangan Kimia
| Rumus | [A]m+[B]n⇔[C]p+[D]q |
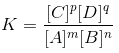
Kesetimbangan Heterogen
Pada bentuk zat dalam reaksi yang terlibat dikesetimbangan heterogen ini tidak sama, maka yang diambil untuk menentukan tetapan kesetimbangan yakni konsentrasi zat yang tetapan kesetimbangannya dipengaruhi yaitu larutan dan gas.
Kesetimbangan Homogen
Pada kesetimbangan homogen ini bantuk zat-zat yang terlibat pada reaksi sama, jadi seluruh konsentrasi zat dipakai untuk menentukan tetapan kesetimbangan.
Ciri Kesetimbangan Kimia
Tidak semua reaksi akan langsung mencapai titik kesetimbangannya, berikut ini merupakan karakteristik suatu reaksi kimia dapat dikatakan telah mencapai kesetimbangan, antara lain;
- Reaksi dalam sistem setimbang terjadi dalam dua arah berlawanan dan berlangsung tanpa henti (dinamis)
- Laju reaksi ke kanan (reaksi maju) harus sama dengan laju reaksi ke arah kiri (reaksi balik)
- Kesetimbangan kimia hanya dapat terjadi dalam sistem tertutup
- Tidak terdapat perubahan yang dapat dilihat secara makroskopis dalam sistem reaksi tersebut
- Katalis tidak berpengaruh dalam kesetimbangan, sebab hanya berperan dalam mempercepat laju reaksi
Faktor Yang Mempengaruhi Kesetimbangan Kimia
Terjadinya kesetimbangan kimia dalam suatu reaksi dipengaruhi oleh beberapa faktor sebagai berikut;
Perubahan Konsentrasi
Berdasarkan prinsip Le Chatelier penambahan reaktan dalam sistem yang telah setimbang akan menggeser reaksi untuk bergerak ke arah kanan (ke arah produk) dan sebaliknya untuk pengurangan konsentrasi reaktan akan menggeser reaksi ke arah kiri (ke arah reaktan).
Hal yang sama juga berlaku pada produk, penambahan konsentrasi produk akan menyebabkan reaksi bergeser ke arah reaktan dan pengurangan produk akan menggeser reaksi ke arah produk.
Dalam sektor industri, faktor ini dapat dimanfaatkan untuk mencapai tingkat konversi produk yang tinggi dan efisien dengan mengarahkan reaksi ke arah produk atau kanan.
Perubahan Tekanan
Perubahan tekanan atau volume dalam sistem juga akan mengganggu sistem kesetimbangan yang sudah terbentuk. Ketika tekanan sistem meningkat atau volume berkurang, maka kesetimbangan akan bergeser ke sisi yang jumlah molnya lebih sedikit dan ketika tekanan berkurang atau volume meningkat, maka kesetimbangan akan bergeser ke sisi yang jumlah molnya lebih banyak.
Dalam hal ini koefisien reaksi sangat berpengaruh karena koefisien akan menentukan jumlah mol dari suatu zat.
Perubahan Suhu
Pengaruh suhu dalam suatu sistem setimbang berkaitan dengan panas reaksi dimana pada reaksi endoterm, maka panas akan diserap oleh reaksi sehingga akan menghasilkan nilai entalpi reaksi positif.
Ketika suhu sistem dinaikkan, maka kesetimbangan akan bergerser ke sisi yang merupakan reaksi endoterm atau menyerap panas. Akan tetapi apabila suhu diturunkan, maka reaksi akan bergeser ke sisi yang merupakan reaksi endoterm atau melepaskan panas.
Pergeseraan Kesetimbangan Kimia
Dalam reaksi kimia ternyata terjadi pergeseran kesetimbangan. Nah dalam hal ini terjadi disebabkan oleh pengaruh beberapa faktor. Dibawah ini terdapat beberapa faktor yang menyebabkan pergeseran kesetimbangan kimia ialah:
- Konsentrasi zat
Dalam perhitungan reaksi kimia apabila konsentrasi zat ditambah atau dikurangi, maka akan menyebabkan pergeseran pada kesetimbangannya. Namun jika konsentrasinya ditambah, maka akan terjadi pergerakan kesetimbangan dan menjauhi zat yang ditambahkan konsentrasinya.
- Tekanan dan Volume
Tekanan dan volume mempengaruhi kesetimbangan kimia. Kemudian disederhankan dengan penjelasan bahwa tekanan dan volume merupakan dua hal yang berbanding terbalik dalam kesetimbangan kimia.
Namun keduanya dapat menyebabkan pergeseran kesetimbangan kimia. Pengaruh tekanaan dan volume terhadap kesetimbangan yaitu:
- Apabila terjadi penambahan tekanan pada suatu sistem maka volumenya diperkecil, akan menyebabkan reaksi kesetimbangan mengalami pergeseran ke arah zat yang jumlah molekulnya lebih kecil, Pergeseran terjadi kearah kanan.
- Begitu juga apabila pada volumenya diperkecil dan diperbesar akan menyebabkan reaksi kesetimbangan bergeser ke arah yang jumlah molekulnya lebi besar, Pergeseran terjaadi kearah kiri.
- Temperatur
Temperatur akan menyebabkan pergeseran kesetimbangan. Temperatur ini berkaitan dengan kalor, sehingga arah pergeseran kesetimbangan kimia adalah pada zat yang menerima (membutuhkan) kalor dan zat yang melepaskan kalor.
Jika temperatur dinaikkan pergesaran kesetimbangan kimia akan menuju ke arah reaksi yang membutuh kalor. Sebaliknya, jika temperatur diperkecil, pergeseraan kesetimbangan kimia akan menuju ke arah reaksi yang melepaskan kalor.
Contoh Soal Kesetimbangan Kimia
Diketahui bahwa suatu reaksi kesetimbangan2A + B <==> A2B
Pada kondisi awal di dalam bejana 2 liter terdapat 2 mol A dan 2 mol B. apabila dalam kesetimbangan 0,5 mol A, jadi berapakah tetapan kesetimbangannya ?
Penyelesaian:
Dari penyataan diatas dapat ditentukan jumlah mol sebagai berikut:
2A+B⇔A²B
Awal 2 2
Reaksi 1,5 0,75 0,75
Setimbang 0,5 0,25 0,75
Maka:
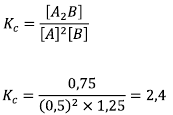
Dalam kasus ini Volume tersebut berpengaruh oleh sebab akan saling menghilangkan
Tetapan kesetimbangan parsial
Tetapan kesetimbangan parsial ialah perbandingan dari hasil kali tekanan pasrsial produk berpangkat kofisiennya masing-masing dengan tekanan pasrsial reaktan berpangkat kofisiennya masing-masing. Tetapan kestimbangan parsial disimbolkan dengan “Kp”.
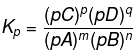
Keterangan:
P = tekanan parsial
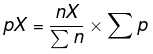
Keterangan:
- pX = tekanan parsial yang akan dicari.
- nX = mol dari zat yang akan dicari tekanan parsialnya.
- En = total mol sistem.
- Ep = total tekanan parsial sistem.
Sekian materi kali ini tentang kesetimbangan kimia, semoga artikel ini menjadi sumber referensi dan menambah wawasan serta pengatahuan bagi sobat semua.
Daftar Pilihan Artiokel Lainnya:

