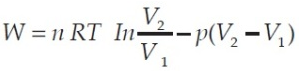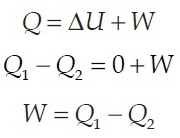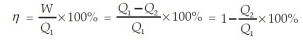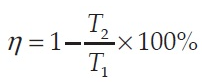Siklus Carnot – Setelah sebelumnya ContohSoal.co.id membahas materi tentang Kalor Jenis. Maka dipertemuan kali ini akan ContohSoal.co.id jabarkan secara detail materi tentang siklus carnot mulai dnari pengertian, ciri, rumus dan contoh soalnya. Nah untuk lebih jelasnya mari langsung aja kita simak bersama ualsan dibawah ini.
Pengertian Siklus Carnot
Siklus carnot ialah merupakan suatu siklus termodinami-ka yang melibatkan proses isotermal, isobarik, dan isokorik. Siklus adalah suatu rangkaian sedemikian rupa sehingga akhirnya kembali kepada keadaan semula.
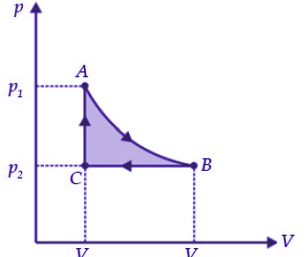
Misalnya, terdapat suatu siklus termodinami-ka yang melibatkan proses isotermal, isobarik, dan isokorik. Sistem menjalani proses isotermal dari keadaan A sampai B, kemudian menjalani proses isobarik untuk mengubah sistem dari keadaan B ke keadaan C.
Hinggga pada hasil akhirnya proses isokorik kembali ke keadaan awalnya (A). Yang membuat dari proses A ke keadaan B, selanjutnya dari C, kembali ke keadaan A, menyatakan suatu siklus.
Jika pada siklus tersebut dapat berlangsung secara terus menerus, maka kalor yang diberikan bisa diubah menjadi sebauh usaha mekanik.
Kalor yang dapat diubah menjadi usaha hanya pada bagian yang diarsir (diraster) saja. Berdasarkan diatas besar usaha yang bermanfaat ialah luas daerah ABCA. Secara matematis dapat ditulis seperti berikut.
Usaha bernilai positif jika arah proses dalam siklus searah putaran jam, dan bernilai negatif jika berlawanan arah putaran jarum jam. Dalam perubahan energi ΔU teruntuk hanya satu siklus yang sama dengan nol ( ΔU = 0) sebab keadaan awal sama dengan keadaan akhir.
Siklus Carnot
Berdasarkan percobaan joule diketahui bahwa tenaga mekanik dapat seluruhnya diubah menjadi energi kalor. Tapi, bisakah seluruh energi kalor dapat diubah menjadi energi mekanik? apakah ada sebuah mesin yang dapat mengubah kalor secara keseluruhan menjadi usaha?
Pada tahun 1824, seorang insinyur berkebangsaan Prancis, Nicolas Leonardi Sadi Carnot, memperkenalkan metode baru untuk meningkatkan efisiensi suatu mesin berdasarkan siklus usaha.
Bentuk Siklus Carnot
Proses Pada Siklus Carnot
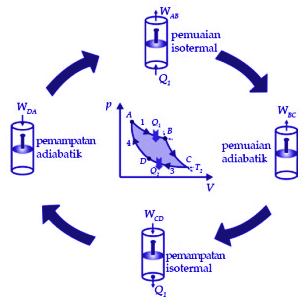
Dari gambar diatas maka bisa jabarkan siklus Carnot sebagai berikut.
- Proses AB ialah merupakan sebuah pemuaian isotermal dalam suhu T1. Yang mana proses sistem ini dapat menyerap kalor Q1 dari reservoir bersuhu tinggi T1 dan melakukan usaha WAB.
- Proses BC ialah merupakan pemuaian adiabatik. YAng mana pada saat proses ini berlangsung suhu sistem turun dari T1 menjadi T2 sambil melakukan usaha WBC.
- Proses CD ialah merupakan suatu pemampatan isoternal pada suhu T2. Dalam menerima usaha WCD hingga dapat melepas kalor Q2 ke reservoir bersuhu rendah T2.
- Proses DA juga termasuk suatu pemampatan adiabatik. Adanya kenaikan suhu pada saat proses ini berlangsung sistem naik dari T2 menjadi T1 akibat menerima usaha WDA.
Dengan berdasarkan fungsinya siklus Carnot juga termasuk sebuah dasar dari mesin ideal yakni mempunyai efisiensi tertinggi yang selanjutnya disebut mesin Carnot. Pada saat usahanya berlangsung total dilakukan oleh sebuah sistem untuk satu siklus sama dengan luas daerah di dalam siklus pada diagram p – V.
Mengingat selama proses siklus Carnot sistem menerima kalor Q1 bersuhu tinggi dari reservoir T1 yang melepaskan kalor Q2 ke reservoir bersuhu rendah T2, maka usaha yang dilakukan oleh sistem menurut hukum I termodinamika adalah sebagai berikut.
Dalam menilai kinerja suatu mesin, efisiensi merupakan suatu faktor yang penting. Untuk mesin kalor, efisiensi mesin (η) ditentukan dari perbandingan usaha yang dilakukan terhadap kalor masukan yang diberikan. Secara matematis dapat dituliskan sebagai berikut.
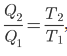
Untuk siklus Carnot berlaku hubungan sehingga efisiensi mesin Carnot dapat dinyatakan sebagai berikut.
Keterangan:
η : efisiensi mesin Carnot
T1 : suhu reservoir bersuhu tinggi (K)
T2 : suhu reservoir bersuhu rendah (K)
Contoh Soal Siklus Carnot
Gas diatomik pada suhu sedang 200ºC dan tekanan 105 N/m2 bervolume 4 lt. Gas mengalami proses isobarik sehingga volumenya 6 liter kemudian proses isokhorik sehingga tekanannya 1.2 x 105 N/m2. Maka Berapakah besarnya pada perubahan energi dalam gas selama proses tersebut ?
Jawab:
PV = n R T ® P DV + V DP = n R DT
Proses A – B (DP = 0):
P DV = n R DT = 105 . 2.10-3 = 200 J
DUBC = 5/2 n R DT = 500 J (diatomik 200ºC)
Proses :B – C (DV = 0):
V DP = n R DT = 6.10-3.0,2. 105 = 1120 J
DUBC = 5/2 n R DT = 300 J (diatomik 200ºC)
Maka total DU=DUAB+DUBC=800 J
Demikianlah materi pembahasan ContohSoal.co.id tentang siklus carnot, semoga artikel kali ini menjadi sajian yang berguna bagi sobat semua.
Artikel Lainnya: