Fraksi Mol – Materi pembahasan kali ini menegnai Fraksi mol lengkap beserta pengertian, rumus dan contoh soal. Namun dipertemuan sebelumnya kami juga telah membahas mengenai Simpangan baku, yuklah langsung aja mari kita simak ulasan dibawah ini.
Pengertian Fraksi Mol

Apa itu Fraksi mol? ialah merupakan satuan konsentrasi yang menyatakan perbandingan antara jumlah mol salah satu komponen larutan (jumlah mol zat pelarut atau jumlah mol zat terlarut) dengan jumlah mol total larutan. Fraksi mol disimbolkan dengan χ . apabila mengandung 2 komponen, yakni zat B sebagai zat terlarut dan A sebagai pelarut, maka fraksi mol A disimbolkan χ A dan χ B untuk fraksi mol zat terlarut.
| Rumus | 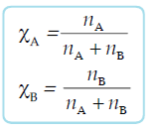 |
| Keterangan |
|
Pada fraksi mol pelarut mempunyai jumlah yang sama dengan 1.
χ A + χ B = 1
Rumus Fraksi Mol
Adapun pengertian Molalitas ialah merupakan konsentrasi larutan yang menyatakan jumlah mol, zat terlarut dalam 1 kilogram atau 1000 gram pelarut. rumus molalitas ialah berikut ini :
Jumlah mol zat pelarut / 1Kg zat pelarut
Zat terlarut (Xt) fraksi mol biasa dirumuskan dengan seperti dibawah ini:
| Rumus | 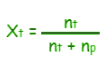
Fraksi mol zat terlarut Xt |
| Keterangan |
|
Fraksi mol zat palarut (Xp) biasa dirumuskan dengan seperti berikut ini:

Hubungan Antara Molalitas Dengan Persen Massa
Persen massa ialah satuan konsentrasi yang juga dapat digunakan didalam larutan kimia. Contohnya ialah larutan yang biasa kita jumpai sehari-hari yaitu larutan alkohol 75% dan larutan asam cuka 24%. Persen masa ialah jumlah gram zat yang terlarut dalam 100 gram massa larutan.
Persamaan yang menunjukkan perhitungan persen massa adalah sebagai berikut :
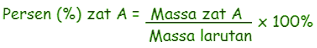
Hubungan Antara Molalitas Dengan Molaritas
Molaritas terlarut dalam satu liter larutan merupakan kandungan sejumlah mol .Kemudian dapat dikonversikan menjadi molalitas, yakni dengan cara merubah volume larutan menjadi massa larutan. Pengubahan volume menjadi massa diperlukan data massa jenis larutan yang dapat dirumuskan sebagai berikut :
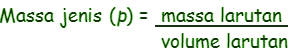
Selanjutnya artian dari Normalitas ialah merupakan besaran yang menyatakan pada jumlah mol ekivalen zat terlarutdidalam tiap satuan volume larutan. Pada Satuan normalitas adalah normal (N) yang = mol ekivalen/liter. Normalitas juga memiliki rumus sebagai berikut :
| Rumus | N = ek/V atau N= n.a/V atau bisa juga N = M x a |
| Keterangan | ek ialah merupakan mol ekivalen yakni jumlah mol dikalikan dengan jumlah ion H+ atau ion OH- |
Sifat Koligatif Larutan
Meski sifat koligatif selalu melibatkan beberapa larutan, namun sifat koligatif tidak bergantung pada interaksi antara zat pelarut dan molekul pelarut , tetapi bergatung pada jumlah zat terlarut yang larut pada suatu larutan . Sifat koligatif itu terdiri dari penurunan tekanan uap juga kenaikan titik didih serta penurunan titik beku dan tekanan osmotik.
Akibat dari Molekul zat cair apabila meninggalkan permukaan maka akan terjadi tekanan uap zat cair. Semakin mudah molekul – molekul zat cair itu berubah menjadi uap, makin tinggi juga tekanan uap zat cair tersebut.
Namun Apabila tekanan zat cair tersebut dilarutkan pada zat terlarut yang tidak menguap, maka partikel – partikel zat terlarut akan mengurangi penguapan molekul zat cair.
Laut mati ialah contohnya dari peristiwa penurunan tekanan uap pelarut oleh zat terlarut yang tidak mudah menguap.
Contoh Soal Fraksi Mol
Agar lebih memahami tentang pengertian dan rumus fraksi mol, maka sebaiknya berlatih soal adalah hal yang paling ampuh, dibawah ini contoh – contoh soal fraksi mol lengkap dengan pembahasannya.
Contoh Soal fraksi Mol 1
Sebuah larutan terdiri dari 3 mol zat A, 3 mol zat B, dan 4 mol zat C.Maka berapakah fraksi mol dari tiap-tiap zat tersebut ?Pembahasan :
Diketahui :
- nA = 3
- nB = 3
- nC = 4
Penyelesaian :
XA = nA / (nA + nB +nC)
XA = 3 / (3 + 3 + 4)
XA = 0.3
XA = nA / (nA + nB +nC)
XA = 3 / (3 + 3 + 4)
XA = 0.3
XA = nA / (nA + nB +nC)
XA=4/(3+3+4)
XA = 0.4
Jadi total dari XA + XB + XC = 0.3 + 0.3 + 0.4 = 1
Contoh Soal fraksi Mol 2
Sebanyak 27,6 gram etanol C2H5OH dilarutkan dalam 54 gram air (Ar C = 12, H = 1, O = 16). Hitunglah fraksi mol etanol dan fraksi mol air!
Penyelesaian:
Diketahui:
massa C2H5OH = 27,6 gr
massa H2O = 54 gr
- Ar C = 12
- Ar H = 1
- Ar O = 16
Ditanyakan: χ etanol dan χ Air = ?
Jawab:
Yang pertama menentukan Mr dari etanol dan Mr dari air, yakni
- Mr.C2H5OH = 46 gr/mol
- Mr.H2O = 18 gr/mol
Kemudian dapatkan jumlah mol dari etanol dan air tersebut:
- n.C2H5OH = massa/Mr = 27,6 gr/(46 gr/mol) = 0,6 mol Iklan
- n.H2O = massa/Mr = 54 gr/(18 gr/mol)
- n.H2O = 3 mol
χ etanol = n.C2H5OH/(n.C2H5OH + n.H2O)
= 0,6 mol/(0,6 mol + 3 mol)
= 0,6 mol/3,6 mol
χ etanol = 0,167
χ Air = n.H2O/(n.C2H5OH + n.H2O)
χ Air =(0,6 mol + 3 mol)
= 3 mol/3,6 mol
χ Air = 0,833
Perhatikan bahwa jumlah fraksi mol = 1
χetanol+χAir=0,167+0,833=1
Demikianlah materi pembahasan kali ini mengenai fraksi mol, semoga artikel ini dapat bermanfaat.
Artikel ContohSoal.Co.id Lainnya:
